医薬品区分適合性調査申請(E31)の作成方法
1.「医薬品等電子申請ソフト」の申請書の選択より、区分適合性調査申請(E31)を選択
【申請様式の選択】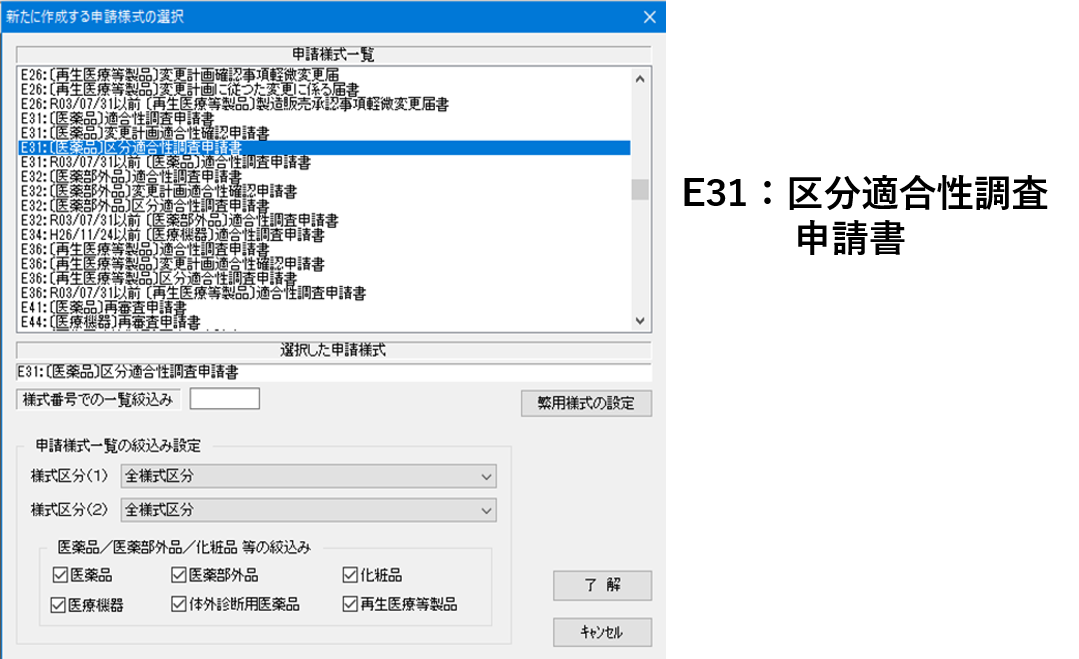
2.「共通ヘッダ」の入力
・提出者の業者コードは、下3桁が「000」のコードを入力すること。
【共通ヘッダ】
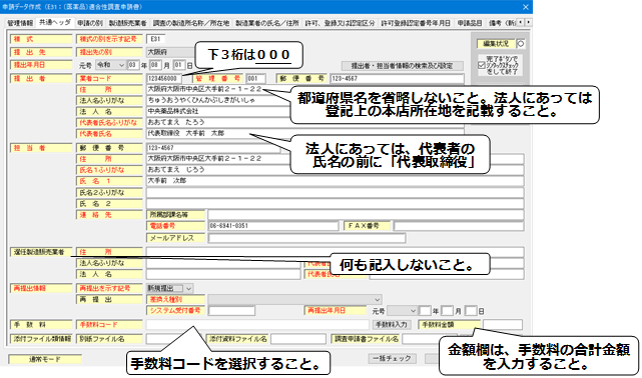
(注意)
手数料については、以下のコードから選択すること
「医薬品基準確認証交付時適合性調査(無菌)」
「医薬品基準確認証交付時適合性調査(一般)」
「医薬品基準確認証交付時適合性調査(包装・表示・保管・試験等)」
「医薬品基準確認証交付時適合性調査(保管製造所)」
【申請の別】
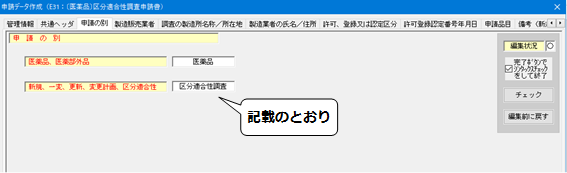
・入力は不要。
5.「調査の製造所名称/所在地」の入力
・製造所の業者コードは、下3桁が「000」以外のコードを入力すること。
・製造所の名称及び所在地は、届出されている最新の内容を入力すること。
【調査の製造所名称/所在地】
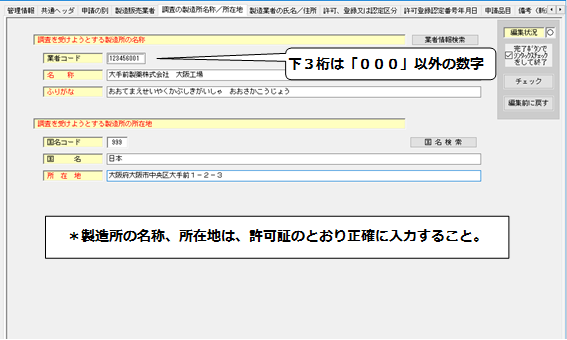
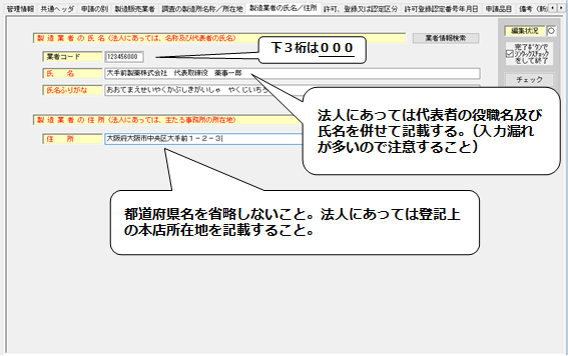
6.「製造業者の氏名/住所」の入力
・製造業者の業者コードは、下3桁が「000」のコードを入力すること。
・「氏名」には、法人にあっては代表者の役職名及び氏名を併せて入力すること。
【製造業者の氏名/住所】
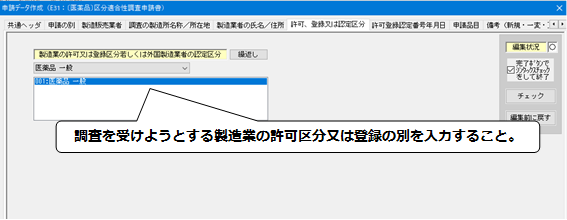
7.「許可、登録又は認定区分」の入力
【許可、登録又は認定区分】
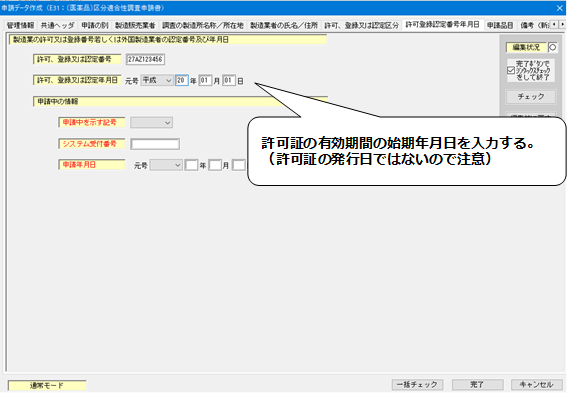
8.「許可登録認定番号年月日」の入力
・許可又は認定年月日には、有効期間の始期年月日を入力すること。
【許可登録認定番号年月日】
9.「申請品目」の入力
・入力不要
10.備考(新規・一変・更新・変更計画)
・入力不要
11.「代行者」の入力
・入力不要(外国製造業者の場合、選定可能な項目の為)
12.「申請する製造区分」の入力
・調査を受けようとする製造工程の区分については、当該製造所における実際の製造工程に合致するものを入力すること。
(手数料コードの説明を参照)
【申請する製造区分】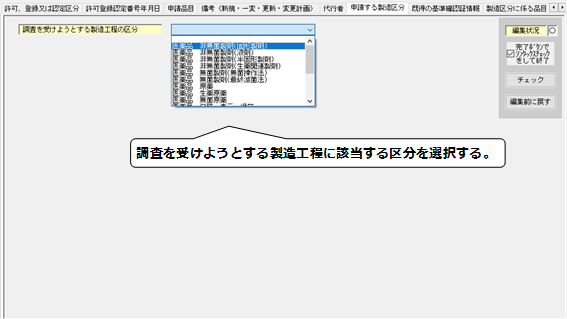
13.「既得の基準確認証情報」の入力
・区分適合性調査を受けようとする製造所が有している基準確認証の情報を入力する。
【既得の基準確認証情報】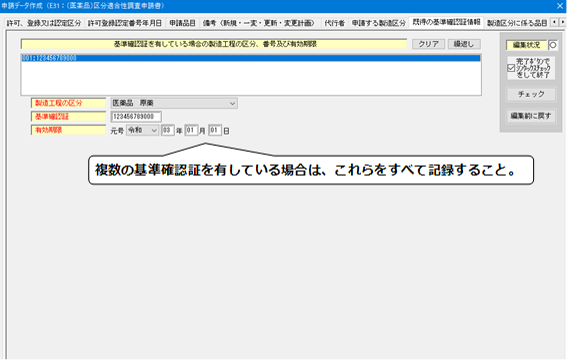
14−1.「製造区分に係る品目」の入力
【製造区分に係る品目】(製剤の場合) 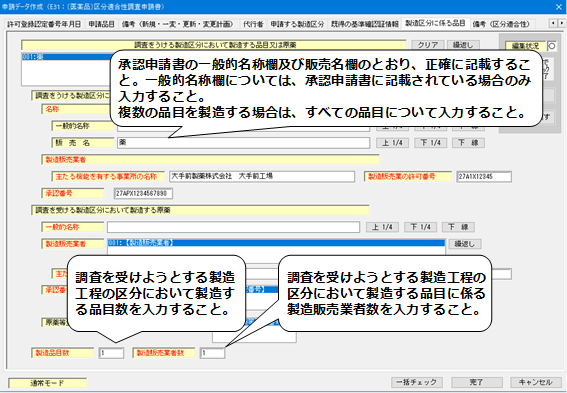
14−2.「製造区分に係る品目」の入力
【製造区分に係る品目】(原薬の場合) 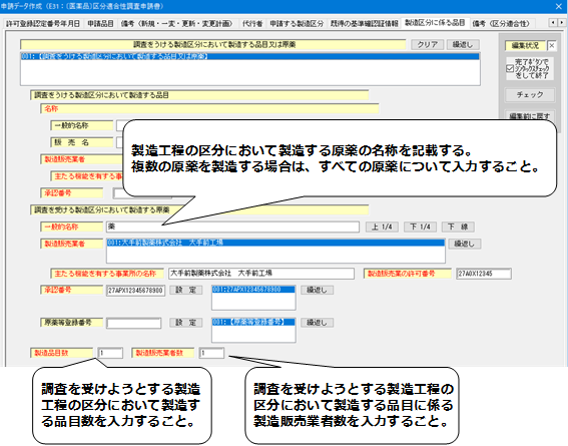
10−3.「備考」の入力:申請要領参照
・手数料の内訳と過去3年間の回収の有無について入力すること。
・手数料の算出が出来るように、一括申請する一物多名称の品目を記載すること。
・調査対象となる原薬名を記載し、その後ろに申請品目名(製剤)を記載すること。
・他に申請中の区分適合性調査申請がある場合は、その申請書のシステム受付番号、製造工程の区分に該当するコード及び申請提出年月日を入力すること。
【備考(区分適合性)】(ほかに申請中の区分適合性がある場合)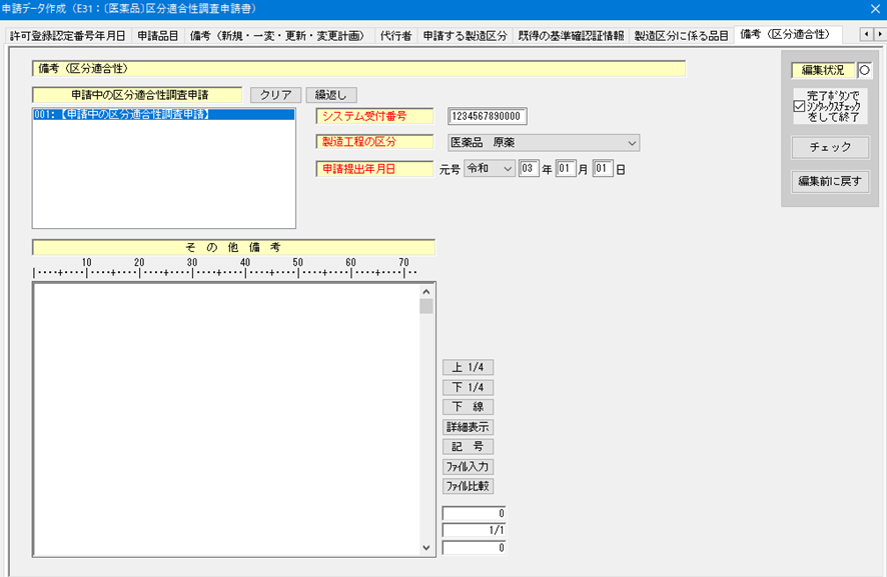
【備考(区分適合性)】(原薬、一物多名称)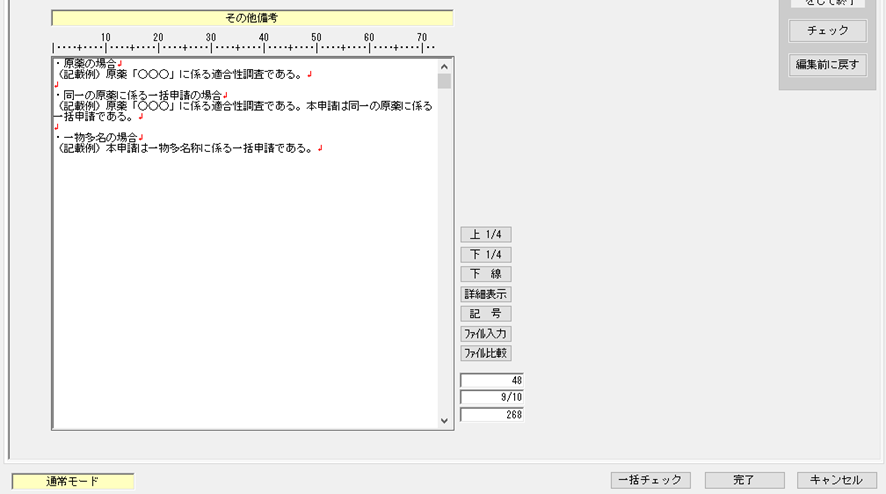
【備考(区分適合性)】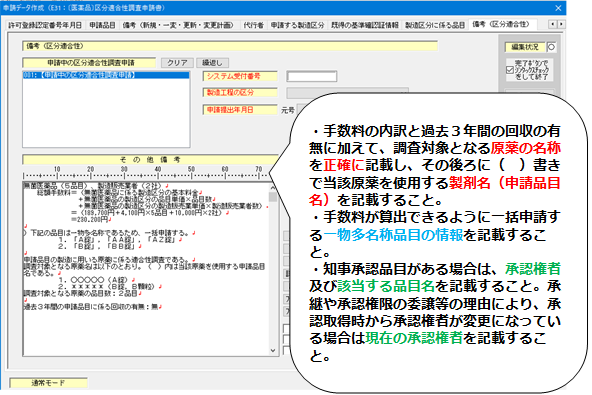
このページの作成所属
健康医療部 生活衛生室薬務課 製造審査グループ
ここまで本文です。

 府庁の組織から探す
府庁の組織から探す